一拖再拖,菲律宾新冠疫苗何时才真正到货。
本帖最后由 ade7788 于 2021-2-22 16:40 编辑
截止周日,菲律宾仍在等待其首批新冠疫苗,菲食药迄今仅向辉瑞与阿斯利康签发紧急使用许可,由中国捐赠的科兴疫苗因未获得菲紧急使用许可可能推迟交货,美国莫德纳公司将申请在菲紧急使用许可。
在原订首批接种疫苗开始日期的一周后菲律宾仍在等待其首批官方新冠疫苗之抵达。
菲律宾总统发言人罗克于二月七日说,首批接种疫苗者——那些前线卫生工作者,将于二月十五日开始。
在二月十二日,疫苗专员加维斯部长说,这些疫苗的抵达将推迟一周,因为本国没有赔偿法律。
目前国会有几项寻求设立为那些由疫苗经历到不利效应的菲人提供赔偿的基金的议案。
在缺乏该法律的情况之下,政府已向辉瑞提交一项赔偿协议以供批准。
在二月十九日,加维斯说他现在不能确定该批疫苗将于二月抵达。
首批疫苗原应是来自世界卫生组织(WHO)领导的COVAX方案的十一万七千剂辉瑞疫苗。
WHO说,该交付将在菲律宾与辉瑞签署一项赔偿协议的两周后发生。
菲律宾食品与药物署(FDA)迄今只向辉瑞与阿斯利康签署紧急用户许可证。
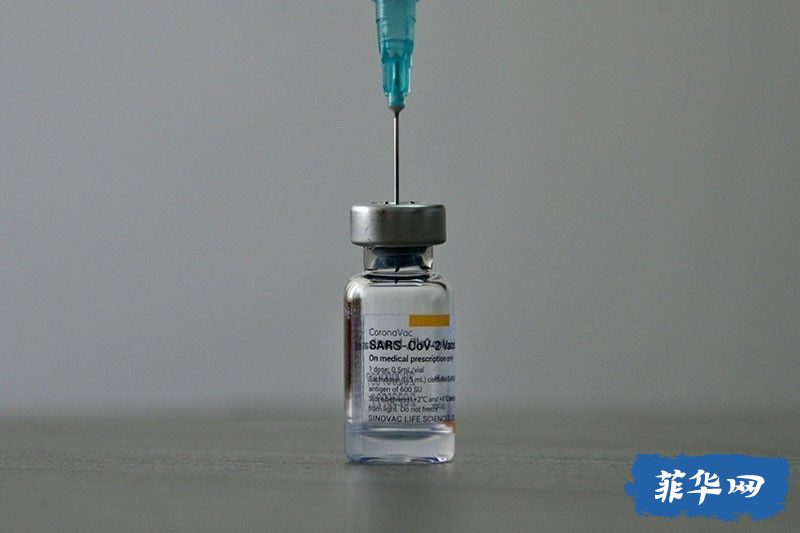
同时,总统府说来自中国公司科兴(SINOVAC)的六十万剂疫苗的二月二十三日预期抵达日期可能因缺乏紧急用户许可证(EUA)而拖延。
由FDA签发的EUA是在菲律宾合法施打疫苗所必需的。
FDA署长多明戈说:“我们不能不加以研究与分析,特别是那科兴疫苗,他们还没有公布他们的数据,它还没有在一种同行重审期刊公布疫苗的内容,例如这是否会发生敏感。”
他又说:“我们只是要特别谨慎,而你知道,谨慎。我们不要等到将来,在如果你加以批准以及已经抵达这里后,我们才开始犹豫。”
此外,FDA又说,我们还不能签发一项EUA给新冠疫苗,SPUTNIK V的制造商GAMALEYA,因为该俄罗斯研究院尚未由FDA取得良好制造做法。
FDA也在等待MODERNA与NOVAVAX的EUA申请。
中国科兴EUA还未批
中国政府已同意捐赠60万剂科兴疫苗,预计将于2月23日抵达。然而,由于在1月13日提交申请后,食药署还没有为科兴颁发紧急使用授权,这可能面临延迟。(最新消息菲食药暑今天已批准颁发中国科兴疫苗紧急使用授权)
莫德纳有意申请EUA
食品和药物管理局(FDA)表示,目前仍在审查中国科兴生物制药(Sinovac Biotech)研发的新冠肺炎(COVID-19)疫苗的数据,审核通过后这些疫苗才能获准在菲律宾紧急使用。
"他们周五下午提交了另一份数据和文件,我会召开会议(与当地卫生专家)来评估这些新数据。"食药局负责人罗兰多·多明戈(Rolando Domingo)在2月21日周日的采访中告诉DZBB电台。
当被问及食药局何时会完成评估时,多明戈表示 "要看情况"。
"这要看情况,因为新数据刚刚到达,我们需要对其进行审查。我们不希望疫苗在信息不全的情况下就在菲使用,特别是在安全和疗效方面。"他说道。
"我们只是想格外小心、尽职尽责。我们不希望疫苗获准使用以后还遇到问题。"他补充说道。
2月11日,总统发言人哈里·罗克(Harry Roque)表示,中国政府将捐赠60万剂科兴新冠疫苗,预计将于2月23日(星期二)抵菲。
不过,罗克2月18日表示,科兴公司已经决定等菲食药局紧急使用授权后,再将疫苗运往菲律宾。科兴公司于1月13日就提交了紧急使用许可申请。
莫德纳疫苗
多明戈表示,美国制药公司莫德纳(Moderna)已经表达了申请EUA的意愿。
"上周我们见面的时候,我问你们什么时候申请?他们说刚完成申请材料,很快就会提交。"他说道。
多明戈表示,由于莫德纳疫苗已经通过了国外严格的监管部门的审核,所以他们对莫德纳疫苗的数据审查起来很容易。
"莫德纳疫苗具有美国等非常严格的监管部门的EUA。在这种情况下,审查起来非常容易,因为书面材料是完整的,甚至美国的评估报告也会提交给我们,所以我们的专家不会重复其他核查问题。"他补充说道。
了解更多请搜索: 菲疫苗
进入原帖,回复讨论
热点关键字
百胜滩旅游攻略, 菲律宾留学怎么样?, 棉兰老旅游攻略, 菲华吧论坛, 海洋公园, 加比地, 菲律宾美食, 佬沃旅游攻略, 菲律宾签证申请, 天使城AngelsCity, 菲律宾工作签证办理, 圣奥古斯丁教堂, 宿务旅游达人攻略, 民多洛旅游攻略, 菲律宾承认双重国籍吗?, 菲律宾马尼拉赌场有那些?, 菲律宾网址导航, 菲律宾签证, 海豚湾旅游攻略, 巴科洛德旅游攻略, 西班牙王城, 菲律宾有哪些大学?, 薄荷岛旅游攻略, 椰子宫, 菲律宾招聘, 菲律宾话费充值, 菲律宾话费充值, 马尼拉教你怎么玩?, 苏比克旅游攻略, 锡基霍尔旅游攻略, 菲律宾旅游签证, 菲律宾交友网站, 菲华吧, 菲律宾结婚, 马尼拉大教堂, 圣地亚哥城堡, 大雅台旅游攻略, 甲米地菠菜岛, 科隆旅游攻略, 公主港旅游攻略, 菲律宾公共假期, 巴拉望旅游攻略, 菲律宾亚航怎么样?, 达卡, 达沃旅游攻略, 八打雁旅游攻略, 美军纪念墓园, 黎刹公园, 黎牙实比旅游攻略, 菲律宾旅游, 菲律宾中文交友, 菲律宾航空怎么样?, 杜马盖地旅游攻略, 菲律宾中文网, 伊洛伊洛怎么样?, 阿普莉, 克拉克旅游攻略, 菲律宾求职, 爱妮岛旅游攻略, 菲律宾宿务航空怎么样?, 菲律宾找工作, 碧瑶旅游攻略, 马尼拉唐人街, 长滩岛怎么样?, 菲律宾虎航怎么样?










